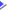前回取り上げたβ-酸化の機構は炭素差に二重結合を含まない飽和脂肪酸にのみ当てはまるものでした。脂肪酸にはこのほか炭素差に二重結合を含む不飽和脂肪酸が有ります。飽和脂肪酸のβ-酸化では4つの酵素が関わりますが、不飽和脂肪酸の場合さらに2つの酵素が必要になります。これは不飽和脂肪酸に二重結合が含まれることが原因です。
β-酸化の経路では一段目にアシルCoAデヒドロゲナーゼと呼ばれる酵素が働き、二段目にΔ(デルタ)2-エノイルCoAヒドロターゼと呼ばれる酵素が働きます。このΔ2-エノイルCoAヒドロターゼはトランス型の二重結合しか反応しません。天然に存在する不飽和脂肪酸の二重結合の多くはシス型となっているため、このままでは不飽和脂肪酸はここでβ-酸化経路の足止めを食らってしまうことになります。そのためこのトランス型の二重結合をシス型に異性化するために別途2つの酵素が必要となるというわけです。
不飽和脂肪酸であるリノール酸を例に不飽和脂肪酸の酸化の過程を見ていきます。まずリノール酸はβ-酸化に入る前に活性化されリノレイルCoAとなります。リノレイルCoAは3回β-酸化のサイクルを通過してcis-Δ3,6ジエノイルCoAとなります。このままではさらにβ-酸化に入ることはできないのでΔ3, Δ2エノイルCoAイソメラーゼによりΔ3の二重結合がシス型からトランス型に変換され、cis-Δ3がtrans-Δ2になります。トランス型になったのでもう一度β-酸化のサイクルに1回入り、さらにβ-酸化の一段目のアシルCoAデヒドロゲナーゼの酵素反応を受けて、trans,cis-Δ2,4ジエノイルCoAとなります。この状態でそのままβ-酸化のサイクルに入ることは出来ないので、ふたたび不飽和脂肪酸の酸化で使われる酵素が必要となります。
まずは2,4-ジエノイルCoAレダクターゼにより二重結合が一つになったtrans-Δ3-エノイルCoAに変換され、さらにΔ3, Δ2エノイルCoAイソメラーゼにより二重結合の位置がずれてtrans-Δ2-エノイルCoAになります。ここまでくれば通常の飽和脂肪酸のβ-酸化の一段目の酵素の反応を受けた後の状態なので、そのままβ-酸化のサイクルに入ることができます。このように不飽和脂肪酸では途中までは普通にβ-酸化のサイクルに入ります。ところがcis型の二重結合の存在があるのでそのままではβ-酸化のサイクルに続けて入れないので、通常のβ-酸化のサイクルに入れるように別の酵素の反応の手助けを得て、形を変えて再びβ-酸化のサイクルに入っていくのです。不飽和脂肪酸でもtrans型のものであればそのままβ-酸化のサイクルに入ることができます。
| 飽和・不飽和脂肪酸の酸化で使う酵素 |
不飽和脂肪酸の酸化で使う酵素 |
アシルCoAデヒドロゲナーゼ
Δ2-エノイルCoAヒドロターゼ
β-ヒドロキシアシルCoAデヒドロゲナーゼ
チオラーゼβ-ケトアシルチオラーゼ
|
Δ3, Δ2エノイルCoAイソメラーゼ
2,4-ジエノイルCoAレダクターゼ
|

■シス型とトランス型
シス型とトランス型の違いは二重結合している炭素に結合している両端の炭素が同じ側にあるものがシス型で、対角線上にあるものがトランス型になります。
■Δ(デルタ)表記
Δ(デルタ)表記は二重結合の位置が何番目にあるのかを示しています。脂肪酸なら例えばΔ9,12と表記されていれば脂肪酸のカルボキシル基(COOH)側やCoA側から数えて9番目と12番目の位置に二重結合があることを示しています。
|
|





 ページTOPへ
ページTOPへ








 脂質
脂質